Pengertian Unsur Kimia & Pengelompokan Unsur Kimia Lengkap – Unsur kimia merupakan sebuah spesies atom dengan jumlah proton yang sama dengan inti atom (nomor atom atau Z yang sama).
Terdapat kurang lebih 118 unsur yang sudah diidentifikasi dan sebanyak 94 unsur di antaranya terbentuk secara alami.
Sebanyak 24 unsur lain adalah sintetis. Setidaknya 80 unsur mempunyai paling sedikit 1 isotop stabil serta 38 unsur adalah radionuklida yang meluruh menjadi unsur lain sejalan dengan waktu.
Pengertian Unsur Kimia & Pengelompokan Unsur Kimia Lengkap
Unsur kimia yang paling banyak menyusun bumi menurut massanya adalah besi dan unsur kimia yang paling banyak di muka bumi adalah oksigen.
Pengertian Unsur Kimia
Unsur kimia ialah sebuah zat kimia yang hanya mempunyai satu jenis atom yang tidak dapat dibagi-bagi lagi menjadi bagian-bagian yang lebih kecil. Atom adalah bagian atau partikel yang paling kecil dari sebuah unsur. Di dalam atom terdapat inti atom (nukleus) yang dikelilingi oleh elektron-elektron.
Inti atom tersusun dari proton dan neutron. Unsur-unsur kimia dalam sistem periodik menurut sifatnya dapat diklasifikasikan menjadi tiga bagian unsur yaitu unsur logam, unsur non logam dan unsur semi logam.
Namun, berdasarkan penemuannya, usnur dibedakan menjadi dua jenis yaitu unsur alami dan unsur buatan.
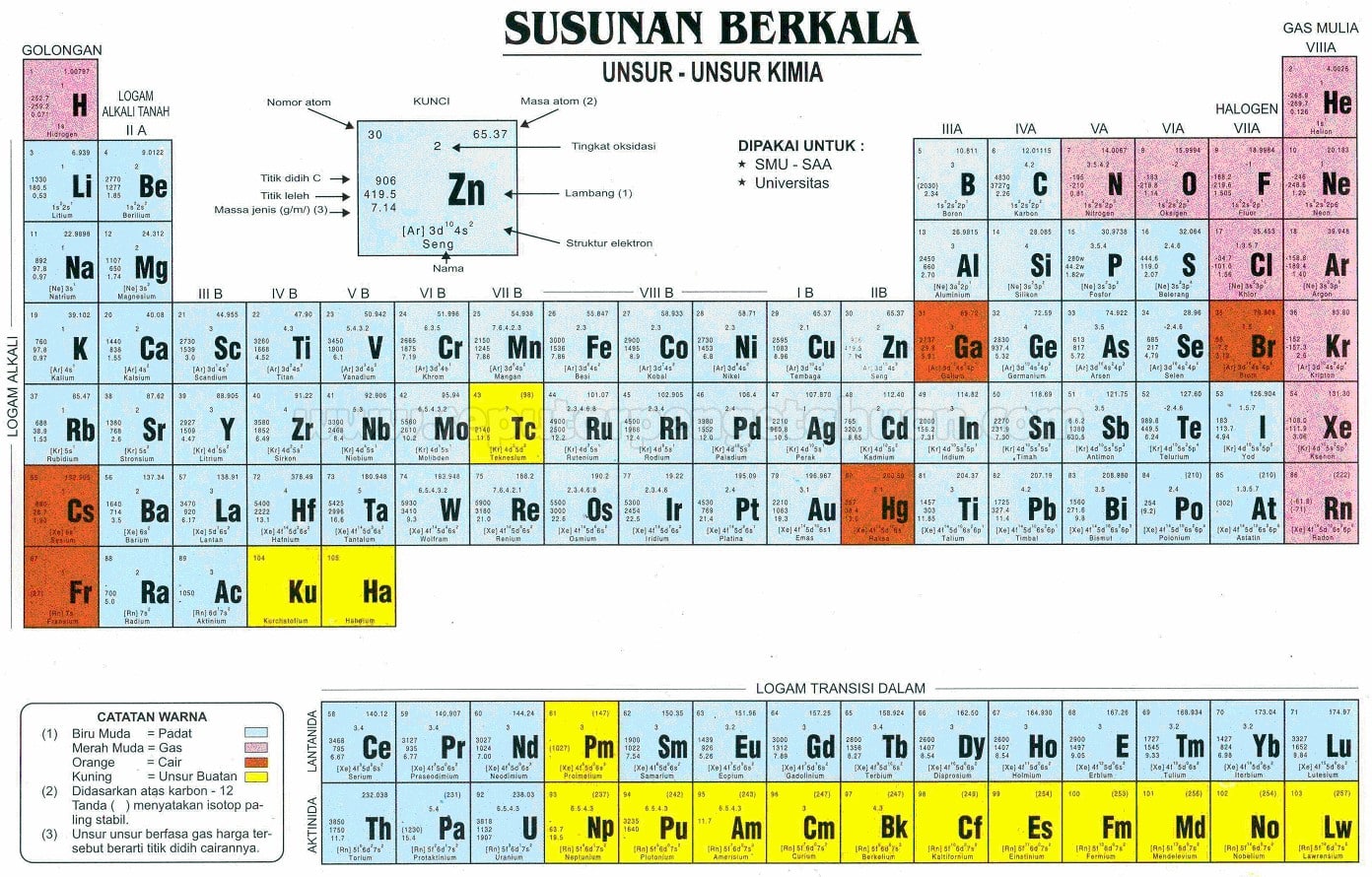
Pengelompokkan Unsur
Unsur pada awanya hanya dibedakan dalam kategori unsur logam dan unsur non logam. Terdapat dua puluh unsur yang ada di masa itu dengan masing-masing unsur mempunyai sifat yang saling berbeda. Teori model atom oleh membuat adanya perkembangan yang cukup signifikan dalam klasifikasi unsur.
Dalam penelitiannya, john Dalton menerangkan bahwa masing-masing unsur memiliki atom-atom dengan sifat-sifatnya tersendiri yang mempunyai perbedaan dengan atom dari unsur-unsur lainnya. Perbedaan tersebut adalah massa unsur.
Semula, massa atom individu belum dapat ditentukan sebab atom memiliki massa yang sangat kecil sehingga digunakanlah massa atom relatif yakni perbandingan massa antar-atom.

Lalu, pada tahun 1814 Berzelius dan P. Dulong serta A. Petit di tahun 1819 melakukan penentuan massa atom relatif menurut kalor jenis unsur. Massa atom relatif merupakan sifat khas pada atom sebab tiap unsur memiliki massa atom relatifnya masing-masing yang tidak sama dengan massa atom relatif unsur-unsur lain.
Penelitian berikutnya di mana Dobereiner, Mendeleev, Newlands serta Lothar Meyer terlibat dalam pengelompokkan unsur menurut massa atom relatif.
Pembeda Sifat Unsur Kimia
Unsur-unsur kimia bisa dikategorikan menurut persamaan sifatnya. Beberapa hal yang menjadi dasar dalam klasifikasi unsur-unsur kimia di antaranya yaitu sifat logam, jumlah kulit elektron dan elektron valensi. Unsur kimia menurut sifat logamnya dibedakan menjadi empat jenis yaitu :
- Logam
- Non logam
- Semi logam
- Gas mulia.
Kemudian, pembagian unsur kimia menurut elektron valensinya dapat dibagi menjadi :
- Golongan utama yang tersusun dari golongan IA, IIA, IIIA, IVA, VA, VIA, VIIA dan VIIIA.
- Golongan transisi yang dibedakan menjadi tiga yakni golongan transisi dalam, lantanida dan aktinida.
Unsur kimia menurut jumlah kulir elektron bisa dibagi menjadi tujuh periode yakni periode 1 sampai periode 7. Unsur-unsur yang berada dalam 1 periode dari kiri ke kanan sifatnya semakin non logam.
Dasarnya unsur kimia bisa dibedakan menjadi dua kategori menurut penemuannya yaitu unsur alami dan unsur buatan. Yang merupakan unsur alami ialah unsur dalam bentuk unsur murni, sedangkan unsur buatan adalah unsur yang dibuat dalam laboratorium dan biasanya berumur pendek.
Unsur Alami
Dari yang telah ditemukan sekitar 116 unsur, 93 unsur di antaranya adalah unsur alami. Salah satu unsur alami yang paling umum keberadaanya di bumi adalah oksigen. Oksigen mempunyai peranan vital sebagai gas untuk pernafasan manusia.
Unsur yang jumlahnya termasuk paling banyak di bumi adalah hidrogen. Unsur-unsur yang terdapat di alam mempunyai lebih banyak senyawa dibandingkan dengan dalam kondisi bebas menurut bentuk dari masing-masing unsur.
Unsur Buatan
Merupakan unsur yang secara alami paling berat. Tetapi, para ilmuwan sudah menciptakan sebuah unsur baru yang mempunyai jauh lebih berat dibandingkan uranium. Penemuan unsur tersebut dilakukan dengan menggabungkan dua unsur kecil bersamaan ddengan kecepatan tinggi.
Tetapi, pada kenyataannya unsur baru tidak dapat tahan lama dan mudah pecah. Para peneliti selalu berupaya agar ubsur baru mampu bertahan lama dengan membuat unsur-unsur dan mempelajari pembentukan serta perubahannya pada saat unsur menjadi lebih berat.
Selain itu, ada juga pembagian unsur menurut sistem periodik unsur yang dibuat oleh imuwan-ilmuwan. Unsut-unsur tersebut adalah unsur logam-unsur no logam dan unsur semi logam.
Unsur Logam
Yang sebagian besar berupa unsur padat dalam suhu dan tekanan normal dengan sifat mengkilap jika digosok dan secara umum dapat ditempa sehingga dapat dibentuk menjadi benda lain dan dapat dijadikan sebagai penghantar panas maupun penghantar listrik. Beberapa contoh unsur logam di antaranya :
- Kalsium (Ca)
- Mangan (Mn)
- Kobalt (Co)
- Timah (Sn)
- Besi (Fe)
- Perak (Ag)
- Krom (Cr)
- Nikel (Ni)
- Kadmium (Cd)
- Kalium (K)
- Emas (Au)
Unsur Non Logam
Adalah unsur dengan wujud gas, cair dan padat dalam suhu dan tekanan normal. Unsur non logam tidak bisa ditempa, tidak bisa digunakan sebagai penghantar panas atau listrik juga tidak bisa mengkilap apabila digosok, terkecuali intan. Beberapa contoh unsur non logam di antaranya :
- Argon (Ar)
- Bromin (Br)
- Belerang (S)
- Helium (He)
- Fluorin (F)
- Fosfor (P)
- Karbon (C)
- Hidrogen (H)
- Oksigen (O)
- Neon (Ne)
- Silikon (Si)
- Nitrogen (N)
Unsur Semi Logam
Dikenal juga dengan nama metaloid. Unsur semi logam (metaloid) adalah unsur yang mempunyai perpaduan sifat dari unsur logam dan unsur non logam.
Umumnya mempunyai sifat semi konduktor artinya bahan yang dapat menghantarkan listrik dengan baik di suhu rendah namun sifat hantaran listriknya akan lebih baik dalam suhu yang lebih tinggi. Beberapa contoh unsur semi logam di antaranya :
- Boron (B)
- Silikon (Si)
- Germanium (Ge)
- Arsen (As)
- Antimony (Sb)
- Tellurium (Te)
- Polonium (Po)
Sekian penjelasan materi Pengertian Unsur Kimia & Pengelompokan Unsur Kimia Lengkap. Terima kasih sudah membaca artikel kami dan semoga artikel ini bermanfaat bagi para pembaca 🙂
